盐碱地改良一定要分清楚盐碱再谈改良,酸碱平衡一定要讲究酸碱的特性!
以下文章来源于梁飞谈水肥 ,作者梁飞 粮肥
盐碱地改良中,如何加酸可以使pH=10的水能够灌溉,和改良盐碱地。中午正在午睡接到一个电话,在睡梦中很多信息都是断片状态,但是醒来后一个信息和内容一直在我脑海中环绕——“有500吨pH10的水,现在因为灌溉需要调整酸碱度到中性,他们选择了柠檬酸和磷酸,根据计算只需要3公斤磷酸。”说实在的我现在也没有搞清楚他们是怎么算的?为了给自己解惑,也给大家答疑,下面我们一起来分析一下这个问题。土壤中存在着各种化学和生物化学反应,表现出不同的酸性或碱性。土壤酸碱性的强弱,常以酸碱度来衡量。土壤之所以有酸碱性,是因为在土壤中存在少量的氢离子和氢氧离子。土壤溶液中的氢离子和氢氧根的构成状况形成了土壤酸碱性,当氢离子大于氢氧根时,称之为酸性;当氢氧根大于氢离子,称之为碱性,用pH值表示。土壤的酸碱性深刻影响着作物的生长和土壤微生物的变化,也影响着土壤物理性质和养分的有效性。我国土壤酸碱性分为七级强酸性(<4.5)、酸性(4.5 ~ 5.5)、弱酸性(5.5 ~ 6.5)、中性(6.5 ~ 7.5)、弱碱性(7.5~8.5)、碱性(8.5~9.5)、强碱性(>9.5)。形成碱性反应的主要机理是碱性物质水解反应产生的OH-,土壤碱性物质包括钙、镁、钠的碳酸盐和重碳酸盐,以及胶体表面吸附的交换性钠。

根据国家标准《水质 PH值的测定 玻璃电极法》(GB 6920-1986)中的定义:对于溶液x,测出伽伐尼电池参比电极1KC1浓溶液H溶液×|H2|pt的电动势EX。将朱知pH(X)的溶液X换成标准pH溶液S,同样测出电池的电动势ES,则pH(X)=pH(S)+(Es—Ex)F/(RTIn10)因此,所定义的pH是无量纲的量。pH没有理论上的意义,其定义为一种实用定义。但是在物质的量浓度小于0.1mo1.dm-3的稀薄水溶液有限范围,既非强酸性又非强碱性(Z<pH<12)时,则根据定义有pH=-Log10[C(H+)y/(mo1.dm3)]±0.02式中C((H+)代表氢离子H+的物质的量浓度,y代表溶液中典型1,—1价电解质的活度系数。当氢离子大于氢氧根时,称之为酸性;当氢氧根大于氢离子,称之为碱性,用pH值表示。测量pH时,按水样呈酸性,中性和碱性三种可能,常配制以下三种标准溶液为了使晶体具有一定的组成,应称取与饱和溴化钠(或氯化钠加蔗糖溶浓(室温)共同放置在干燥器中平衡两昼夜的硼砂(Na2B4O7.10H2O)3.80g,溶于水并在容量瓶中稀释1L。第五、pH10的水中有多少氢氧根,需要多少氢离子呢?pH=10的水中按照强酸强碱溶液计算,溶液中的氢氧根浓度为0.0001;对应的需要的氢离子也是0.0001,需要的酸就是pH=4的酸溶液等量中和。第六、500吨pH10的水中有多少氢氧根,需要多少磷酸中和呢?对于这个关键问题就是500吨氢氧根浓度为0.0001,溶液需要500吨氢离子也是0.0001。简而言之:我们需要500吨pH=4的磷酸。磷酸又叫正磷酸,化学式H3PO4,分子量为97.994,是一种常见的无机酸,是中强酸。磷酸是三元中强酸,分三步电离,不易挥发,不易分解,有一定氧化性。具有酸的通性。pKa1:2.12pKa2:7.21;pKa3:12.67。由于磷酸不是强酸不能完全电离,目前没有见到相关数据,本人2009年做过磷酸脲的溶解性试验,根据我们试验结果40%的磷酸脲溶液的pH≈4.
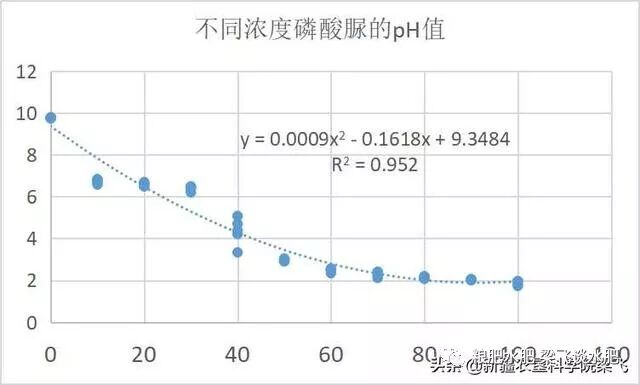
磷酸脲的饱和溶液pH等于1.89;根据资料1%的磷酸大概是pH等于1.5,所以按照系数磷酸不会电解反应计算0.005%的磷酸pH约等于4.也就是说饱和磷酸1公斤可以稀释20吨pH=4的磷酸溶液。500吨对应的应该是25公斤。上面的计算仅仅是理论计算,实际上水中含有大量的钙镁等离子,还有一些有机物质;空气中的二氧化碳一直在平衡中,磷酸还有电离反应,实际上需要远远大于这个数字。具体500吨pH的水需要多少磷酸中和,肯定不是几公斤,应该也不是20公斤,建议做少量的中和试验和中和滴定,在做考虑。总之,盐碱地改良一定要分清楚盐碱再谈改良,酸碱平衡一定要讲究酸碱的特性!